CONTRIBUTO dal Dott. Luigi Ferritto, a scopo divulgativo, Il “Cuore d’Atleta”.
In questi ultimi decenni la cultura sportiva ha subito notevoli cambiamenti. Gli atleti agonisti con importanti ambizioni, infatti, seguono, per la preparazione, rigorose schede d’allenamento che comprendono sedute giornaliere di più ore e che portano a vari adattamenti sia a carico dei muscoli scheletrici, sia a carico del sistema cardiovascolare: proprio i cambiamenti che avvengono su quest’ultimo sono conosciuti come sindrome del “cuore d’atleta”(1). Il lettore, deve però prestate attenzione perché, come su detto, questi adattamenti fisiologici sono propri di atleti di elevato livello agonistico e non di atleti di basso livello o dediti ad attività ludico-ricreativa, dove l’anatomia cardiovascolare non differisce molto dal soggetto sedentario (2).
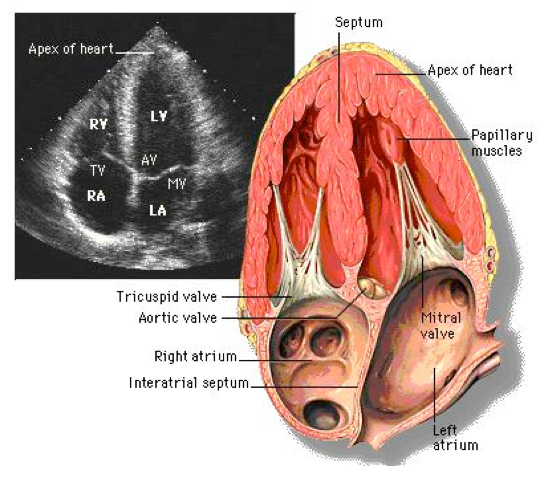
Adattamenti Cardiaci
Gli adattamenti cardiaci sono da sempre i più discussi e studiati, a causa della importanza vitale che ha quest’organo. I lunghi e prolungati allenamenti provocano dei cambiamenti morfologici cardiaci tra cui l’incremento delle dimensioni delle camere cardiache sinistre, del setto interventricolare, della massa e degli apparati valvolari. I meccanismi che provocano modificazioni della morfologia cardiaca negli atleti sono molteplici, ma il tipo di sport ha una particolare importanza: gli sport di resistenza (ciclismo, sci di fondo, canottaggio e canoa) hanno il maggiore impatto nell’ingrandire la cavità ed aumentare lo spessore delle pareti del ventricolo sinistro. Gli atleti praticanti queste discipline presentano dimensioni delle pareti e/o delle cavità ventricolari al di sopra dei limiti normali, tanto da simulare una condizione patologica, quale la cardiomiopatia ipertrofica (quando lo spessore delle pareti è > 13 mm) o la cardiomiopatia dilatativa (quando la cavità ventricolare sinistra è > 60 mm). Il meccanismo causale di un così importante rimodellamento cardiaco è rappresentato dall’aumento della portata cardiaca (che durante sforzo supera i 30 l/min) e della pressione arteriosa sistolica (che durante sforzo supera i 200 mmHg).

La dilatazione della cavità ventricolare sinistra negli atleti, soprattutto quelli praticanti sport di resistenza, può arrivare sino a 70 mm, che verosimilmente rappresenta il limite fisiologico dell’ingrandimento indotto dall’allenamento. L’ingrandimento della camera ventricolare avviene in modo globale ed omogeneo, per cui la normale geometria ventricolare non è alterata, così come lo spessore delle pareti è normale o aumentato. Nella cardiopatia dilatativa, anche se le dimensioni assolute della cavità ventricolare possono presentare valori simili all’atleta, non raramente il diametro traverso diastolico supera i 70 mm ed è associata ad un rimodellamento geometrico ventricolare, che tende ad assumere un aspetto globoso. Gli atleti praticanti sport di potenza (sollevamento pesi o lanci) presentano un ispessimento delle pareti ventricolari, che è conseguenza del carico di pressione cui vanno incontro durante l’allenamento (la pressione sistolica supera abitualmente i 200 mmHg, talora anche i 300 mmHg), mentre la cavità ventricolare sinistra non si modifica sensibilmente.
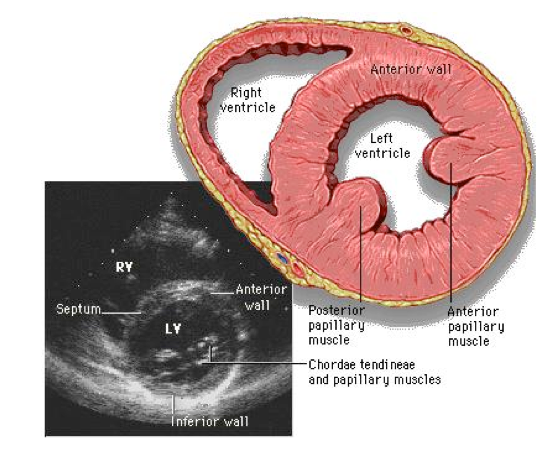
Generalmente, l’ispessimento delle pareti ventricolari negli atleti ben allenati non supera i 15-16 mm, che rappresentano il limite dell’ipertrofia fisiologica indotta dall’allenamento. Nel cuore d’atleta la distribuzione dell’ipertrofia è simmetrica e regolare anche se i diversi segmenti del miocardio ventricolare possono non essere ispessiti in modo uguale (il setto anteriore mostra generalmente il massimo ispessimento) ma le differenze sono modeste e nell’insieme l’ipertrofia risulta simmetrica ed omogenea. Al contrario, nei pazienti con cardiopatia ipertrofica, l’ipertrofia è tipicamente asimmetrica e, anche se il setto interventricolare è la regione più spesso coinvolta dall’ipertrofia, esiste una eterogeneità morfologica e non sono rari i casi in cui il massimo ispessimento interessa solo altri segmenti del ventricolo. Gli atleti praticanti sport di squadra, infine, presentano variazioni della morfologia cardiaca usualmente più lievi, a ragione del carico emodinamico più modesto (3). Il sesso ha importanza nel determinare il grado di rimodellamento cardiaco. Le atlete, quando paragonate ai maschi della stessa età e praticanti le stesse discipline sportive, presentano dimensioni minori sia della cavità (circa – 10%) che dello spessore delle pareti ventricolari (circa – 20%). Queste differenze sono legate ad una serie di fattori, tra cui i principali sono la taglia corporea (e la percentuale di massa magra) mediamente più piccole nelle donne, l’aumento più modesto della portata cardiaca e della pressione arteriosa sistolica durante lo sforzo e, non ultimo, il più basso livello di ormoni androgeni naturali. Le differenze nella morfologia cardiaca tra atleti ed atlete hanno notevole importanza clinica: infatti gli uomini possono sviluppare una ipertrofia delle pareti ventricolari sino a 15 o 16 mm, mentre al contrario le donne raramente superano gli 11 mm. Pertanto, il problema della diagnosi differenziale tra “Cuore d’Atleta” e cardiomiopatia ipertrofica non si pone usualmente nelle atlete (4,5,6). La frazione di eiezione ventricolare sinistra del “Cuore d’Atleta”, misurata ecocardiograficamente o con altre metodiche, risulta uguale o leggermente inferiore alla norma; al contrario, la funzione diastolica è nettamente aumentata e migliorata negli atleti, tanto che il riempimento ventricolare appare già completo in protodiastole e ciò sembra strettamente associato ad un incremento delle dimensioni e delle performance cardiache. Caratteristiche del ventricolo sinistro nel “Cuore d’atleta” sono delle trabecole fibrose o fibro-muscolari tese tra le sue pareti, definite false corde tendinee per differenziarle dalle vere corde: generalmente sono tese tra setto interventricolare e parete laterale, in vicinanza dell’impianto dei muscoli papillari. Anche l’atrio sinistro, che riceve il sangue ossigenato dai polmoni, non è esente da modificazioni morfologiche, infatti negli atleti di fondo non è difficile evidenziare un ingrandimento superiore alla norma (40 mm) (7). Analogamente le camere cardiache di destra subiscono un aumento proporzionato del volume.

Un altro aspetto importante è il riscontro relativamente frequente negli atleti di rigurgiti valvolari “fisiologici” possibili in corrispondenza di tutte e quattro le valvole cardiache, ma con frequenza estremamente variabile e in assenza di alterazioni strutturali (8). La prevalenza dei questi rigurgiti sembra legata all’aumentare del tempo di allenamento, sembra associata al fisiologico ingrandimento delle camere cardiache e generalmente sono senza alcun significato emodinamico (9,10,11). Raramente un ecocardiografista esperto non è in grado di effettuare una diagnosi differenziale tra una insufficienza valvolare fisiologica e patologica.
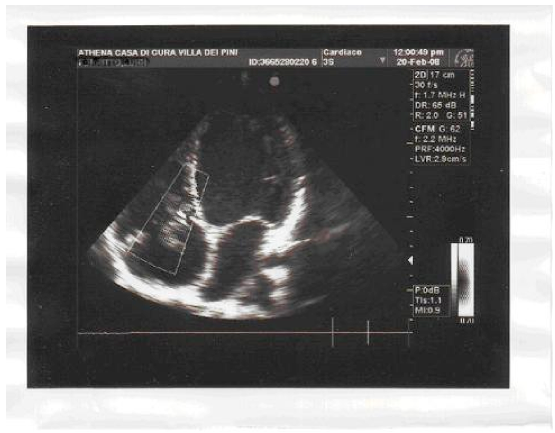
Nelle insufficienze “fisiologiche”:
- è assente qualsiasi alterazione strutturale valvolare,
- non si osservano fenomeni di turbolenza ed aliasing al Doppler,
- l’area di rigurgito è limitata alla zona mediana immediatamente sottovalvolare, con rilievo del segnale
Doppler fino e non oltre a 1-2 cm da essa.
All’esame fisico, un soffio meso-sistolico o (olo) sistolico, di intensità 1-2/6 può essere ascoltato fin nel 50% degli atleti ( 12): probabilmente riflette il flusso non laminare attraverso le valvole aortica e polmonare, secondario all’aumento della gittata sistolica e spesso diminuisce d’intensità al passaggio dalla posizione supina a quella ortostatica (13). Recentemente è stato suggerito che il rimodellamento cardiaco possa essere regolato anche da fattori genetici e costituzionali. Sebbene tale ipotesi sia assai attraente, al momento esiste una conferma solo per quanto riguarda l’enzima ACE (che controlla il livello della pressione arteriosa e può presentarsi nelle isoforme DD, II e ID) ed altri enzimi del sistema renina-angiotensina-aldosterone. E’ stato dimostrato che i soggetti che hanno il pattern ACE di tipo DD sviluppano una massa ventricolare sinistra maggiore in confronto a quelli con pattern II (14).

Adattamenti Periferici
È logico che anche il sistema circolatorio, costituito da vasi arteriosi e venosi, debba adattarsi a questa nuova realtà. In altri termini, la circolazione deve essere potenziata al fine di consentire lo scorrimento di flussi sanguigni (equivalenti al traffico automobilistico) così elevati senza “rallentamenti”. A seguito dell’allenamento di resistenza, si ha un aumento delle arterie coronarie che nutrono il cuore. Il cuore dell’atleta, aumentando il suo volume e la massa muscolare, ha bisogno di un maggior rifornimento di sangue e di una maggiore quantità di ossigeno. L’aumento del calibro delle coronarie (i vasi che nutrono il cuore) costituisce un altro degli elementi che differenziano l’ipertrofia fisiologica del cuore da quella patologica legata alle malattie cardiache congenite o acquisite. I vasi arteriosi e venosi di medio e grosso calibro aumentano le loro dimensioni (“vasi d’atleta”): questo fenomeno è particolarmente evidente nella vena cava inferiore, il vaso che riporta al cuore il sangue proveniente dai muscoli degli arti inferiori, utilizzati molto nei vari sport. A carico della microcircolazione, gli adattamenti più importanti riguardano naturalmente i muscoli (particolarmente i muscoli più allenati). I capillari, attraverso i quali avvengono gli scambi tra sangue e muscolo, sono distribuiti in maggior misura attorno alle fibre muscolari rosse, lente, a metabolismo aerobico (fibre ossidative), che hanno bisogno di una maggiore quantità di ossigeno (15). Nell’atleta di resistenza con l’allenamento si realizza un aumento in assoluto del numero di capillari e del rapporto capillari / fibre muscolari. Tale fenomeno è conosciuto con il nome di capillarizzazione e grazie ad esso, le cellule muscolari vengono a trovarsi nelle migliori condizioni per sfruttare a pieno le aumentate disponibilità di ossigeno e substrati energetici. L’aumento della superficie capillare e della capacità di vasodilatazione delle arteriole muscolari, fa sì che i muscoli riescano ad accogliere quantità di sangue veramente notevoli senza che aumenti la pressione.
Training e Detraining
In numerosi studi, la valutazione ecocardiografica dell’ipertrofia ventricolare sinistra ha dimostrato che, sia nel corso del periodo di allenamento (training), che dopo la sua interruzione (detraining), possono verificarsi modificazioni molto rapide delle dimensioni e dell’ipertrofia del ventricolo sinistro. In tempi relativamente brevi, sia i fondisti (osservati per 7 settimane), che i nuotatori (osservati per 10 settimane), hanno presentato rapide modificazioni sia delle dimensioni che dell’ipertrofia ventricolare, con aumenti delle dimensioni cavitarie sinistre sino a 15 mm al termine dello studio. Durante la fase di detraining, sia i nuotatori che i fondisti hanno evidenziato un progressivo ridimensionamento delle dimensioni telediastoliche delle cavità cardiache sinistre. Non è ancora accertato se le più evidenti modificazioni osservate negli atleti di resistenza progrediscano rapidamente, ma è possibile che, dopo un lungo periodo di adattamento, tali modificazioni regrediscano molto più lentamente (16).
Valutazione del ritmo cardiaco dell’atleta
Lo studio dell’elettrocardiogramma dell’atleta ha sempre appassionato i cardiologi fin dalle prime interpretazioni dell’elettrocardiografia. Molte sono le modificazioni dell’elettrocardiogramma descritte negli atleti e spesso considerate innocente effetto dell’allenamento; tuttavia alcune modificazioni, quali l’aumento marcato di voltaggio delle onde R o S, un sopraslivellamento del tratto ST, l’inversione dell’onda T, la presenza di onde Q profonde, suggerisce la presenza di una cardiomiopatia ipertrofica o cardiomiopatia aritmogena del ventricolo destro.
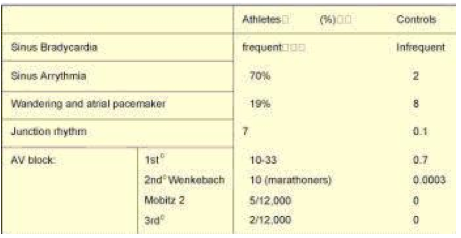
Al momento attuale il significato clinico di tali alterazioni in atleti peraltro sani, non è ancora ben definito, non è chiaro cioè se tali anomalie ECG siano la prima espressione di una cardiomiopatia che si svelerà in un tempo successivo, oppure siano semplice espressione del rimodellamento morfologico cardiaco indotto dall’allenamento. In realtà solo una piccola percentuale di atleti che mostrano alterazioni marcate dell’ ECG presentano, alla verifica ecocardiografica, anomalie mentre la maggioranza sono risultati “falsi positivi”(17) . Numerosi sono stati gli studi epidemiologici condotti sulla prevalenza delle diverse aritmie cardiache negli sportivi. Tra le aritmie più frequenti negli atleti rispetto alla popolazione sedentaria si evidenzia: le bradicardie sinusali, i ritardi di conduzione atrioventricolare e le tachiaritmie.
La Bradicardia sinusale
La bradicardia sinusale è l’espressione peculiare dell’elettrocardiogramma dello sportivo ed è talora caratterizzata da valori a riposo anche inferiori ai 40 bpm. E’ più frequente negli atleti praticanti sport di resistenza ad elevato livello agonistico. Generalmente, la bradicardia sinusale, se non accompagnata da sintomatologia sincopale e se normalizzata dall’esercizio fisico, è inquadrata nel cosiddetto adattamento “ipervagotonico” all’allenamento fisico intenso e, nella maggioranza dei casi, non pone problemi di idoneità allo sport agonistico intenso. Molti studi hanno documentato che un allenamento intenso e duraturo è in grado di modificare l’equilibrio simpatovagale in senso vagale, inducendo la predominanza della componente parasimpatica. Tale effetto è particolarmente evidente in quelle regioni cardiache che maggiormente risentono della prevalenza del tono vagale come il nodo del seno ed il nodo atrioventricolare. E’ probabile che alcune bradicardie molto marcate siano l’espressione anche di una componente genetico-costituzionale e vadano seguite attentamente nel tempo. Le bradicardie estreme dell’atleta devono essere distinte dalle bradicardie espressione di una iniziale disfunzione sinusale, soprattutto in età adulta e avanzata, nella quale l’evenienza di una malattia del nodo del seno è cronologicamente più probabile.
Ritardi della conduzione atrioventricolari
L’ipervagotonia indotta dall’allenamento può essere considerata il primum movens patogenetico anche per queste forme di bradiaritmia. Si tratta generalmente di blocchi atrioventricolari di 1° grado o di 2° grado tipo Mobitz 1, con espressione tipicamente notturna e con completa normalizzazione dopo test da sforzo massimale o dopo periodo di disallenamento.
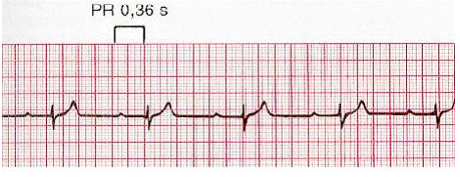
Una particolare attenzione deve essere posta ai casi di blocco atrioventricolare già evidente in giovane età che non si associano ad un intenso condizionamento fisico o ai casi presenti in età adulta, soprattutto se si tratta di blocco atrioventricolare di grado avanzato od associato a blocco di branca.
Tachiaritmie-Aritmie sopraventricolari
La prevalenza dei battiti prematuri sopraventricolari nell’atleta è molto variabile (intorno al 30%) da casistica a casistica e generalmente non assume rilevanza clinica né compromette l’idoneità all’attività sportiva agonistica. Di interesse maggiore sono le varie forme di tachicardia parossistica, di flutter o di fibrillazione atriale parossistica. Nello sportivo tali tachiaritmie rappresentano un importante problema, in seguito al cardiopalmo che provocano, soprattutto quando tale sintomo accade durante lo sforzo fisico. Per fortuna questi episodi sono molto rari nello sportivo con una prevalenza del 1%. Il sintomo del cardiopalma nell’atleta è sostenuto dalle seguenti aritmie: tachicardia da rientro atrioventricolare (50%); fibrillazione atriale (25%); flutter atriale (13%); tachicardia da rientro atrioventricolare da via anomala occulta e tachicardia atriale (6,2%).
Aritmie ventricolari
Le aritmie ventricolari nell’atleta apparentemente sano rappresentano una delle tematiche più controverse in ambito della cardiologia dello sport. Tale problematica può essere riassunta in alcuni punti fondamentali:
- la prevalenza di battiti ectopici ventricolari isolati nello sportivo è molto frequente stimabile tra il 35% e il 50%
- È spesso difficile identificare un substrato organico come causa dell’aritmia, anche nelle forme più maligne
- Non esistono ancora studi longitudinali per poter stabilire un follow-up adeguato.
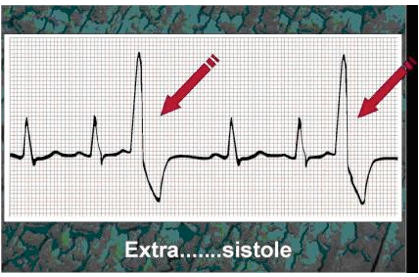
Sono sempre più frequenti gli studi che documentano la presenza di un substrato organico associato all’aritmia come minime anomalie a carico dell’infundibolo ventricolare destro, miocarditi in fase di remissione, cardiopatia aritmogena del ventricolo destro ed altre forme minori di cardiopatia. In tal senso lo sforzo fisico è generalmente inquadrabile come fattore scatenante od aggravante l’aritmia.
Sulla base di queste osservazioni è utile proporre un iter valutativo dell’atleta con aritmie ventricolari, articolato nei seguenti punti:
- scrupolosa ricerca di una cardiopatia organica associata all’aritmia,
- attento studio aritmologico degli atleti sintomatici (per sincope o cardiopalmo),
- cautela nell’indicazione e prescrizione di metodiche invasive negli atleti aritmici asintomatici, nei quali manca un vero end-point elettrofisiologico, a causa della difficoltà di attribuire ad una aritmia inducibile, potenzialment aspecifica, un rischio reale di morte improvvisa
- vale la pena sottolineare che tra le forme più pericolose rientrano proprio quelle aritmie ventricolari che, per assenza di ripercussioni sulla performance, consentono di praticare lo sport ad alto livello, esponendo l’atleta ad un reiterato rischio.
Negli atleti andranno considerate in modo benigno quelle forme “occasionali” di aritmie ventricolari, non ripetibili e non associate allo sforzo fisico (18) .
Screening Cardiologico Preventivo
L’esercizio fisico, come su ampiamente descritto, può scatenare eventi acuti cardiovascolari, tra i quali i più temibili sono la morte improvvisa e le sindromi coronariche acute. La probabilità che si verifichino eventi cardiovascolari durante esercizio fisico è più elevata nei pazienti affetti da cardiopatia, nei soggetti in età adulta/avanzata, in quelli sedentari e con fattori di rischio cardiovascolare e quando l’attività fisica è praticata ad intensità elevata. La probabilità, invece, è minore quando l’attività fisica è praticata a bassa intensità e nei soggetti che si allenano regolarmente. Il meccanismo attraverso cui l’attività fisica abituale esercita questo effetto protettivo nei confronti degli eventi acuti cardiovascolari ed in particolare della morte improvvisa, è legato probabilmente ad una maggiore stabilità elettrica del miocardio, con riduzione del rischio di aritmie ventricolari fatali. Allo scopo di ridurre il rischio di eventi cardiaci avversi, quindi, risulta importante eseguire un adeguato screening preventivo ed avviare i soggetti ad un graduale e progressivo condizionamento fisico, soprattutto se hanno cardiopatia nota, età avanzata, o fattori di rischio coronario (19). Ogni individuo, quindi, che si accinge ad iniziare una attività fisica regolare, dovrebbe essere sottoposto, preventivamente, ad una attenta valutazione cardiologia che deve essere ancora più accurata in caso di atleti, visto i grossi carichi di lavoro effettuati. E’ pensiero comune che attraverso un adeguato screening preventivo, si possa ridurre la probabilità di eventi cardiovascolari avversi, in modo da godere dei benefici dell’attività fisica senza incorrere nei rischi ad essa associati. Scopo dello screening preventivo è quello di scovare l’esistenza di cardiopatie clinicamente silenti in soggetti apparentemente sani, nonché in caso di cardiopatia clinicamente accertata, stratificare il rischio associato alla pratica dell’attività sportiva ed attivare gli interventi terapeutici necessari (20).
Conclusioni
Negli ultimi anni si è verificato un enorme incremento della popolarità di molti sport. Ne è derivato un aumento del numero di soggetti che giungono all’osservazione del medico presentando gli effetti cardiovascolari dell’allenamento. La conoscenza delle modificazioni cardiovascolari negli atleti è essenziale per evitare erronee diagnosi di cardiopatia.
Dott. Luigi Ferritto
Dipartimento di Medicina Generale
Ambulatorio di Fisiopatologia dello Sport
